what is heisenberg uncertainty principle
हाइज़नबर्ग की अनिश्चितता सिद्धांत: यह क्यों संभावना नहीं है कि हम एक वस्तु के स्थान और गति दोनों को एक साथ सटीकता से माप सकें
हाइज़नबर्ग की अनिश्चितता सिद्धांत क्या है?
हाइज़नबर्ग की अनिश्चितता सिद्धांत का कहना है कि किसी वस्तु के स्थान और गति को एक साथ सटीकता से मापना या गणना असंभव है। इस सिद्धांत का मूल आधार पदार्थ के तरंग-कण द्वैतीयता पर है।
जर्मन भौतिक विज्ञानी वेर्नर हाइज़नबर्ग ने 1927 में इस सिद्धांत का प्रस्ताव किया था, जिसमें कहा गया है कि किसी कण के स्थान और गति को एक साथ मापने में मौलिक सीमाएँ होती हैं।
यह क्यों संभावना नहीं है कि स्थान और गति दोनों को एक साथ मापा जा सके?
किसी वस्तु के स्थान को मापने के लिए, एक फोटॉन को उसके साथ टकराना होता है और यह मापन उपकरण में वापस आता है। क्योंकि फोटॉन में कुछ निर्धारित गति होती है, फोटॉन जब इलेक्ट्रॉन के साथ टकराता है, तो गति का संचालन होता है।
इस गति के संचालन के कारण इलेक्ट्रॉन की गति बढ़ जाती है। इस प्रकार, किसी कण के स्थान को मापने का कोई भी प्रयास किया जाता है, तो उसकी गति के मापन में अनिश्चितता बढ़ जाती है।
हाइज़नबर्ग की अनिश्चितता सिद्धांत का सूत्र और अनुप्रयोग
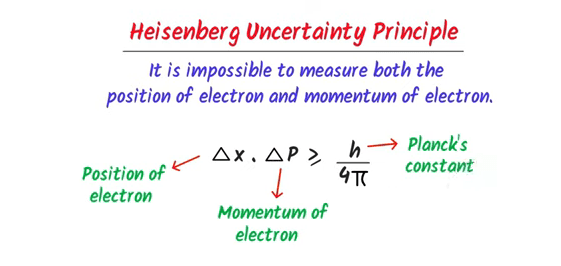
हाइज़नबर्ग की अनिश्चितता सिद्धांत का सूत्र निम्नलिखित है:
जहाँ:
= स्थान मापन में त्रुटि
= गति मापन में त्रुटि
= प्लांक स्थिरांक (6.626 × 10^-34 Js)
यह सिद्धांत हमें यह बताता है कि स्थान और गति के मापनों में अनिश्चितता का गुणनफल हमेशा एक न्यूनतम मान से अधिक होता है।
एक उदाहरण के साथ हाइज़नबर्ग की अनिश्चितता सिद्धांत की व्याख्या
एक परमाणु में एक इलेक्ट्रॉन का मास 9.91 × 10^-31 किलोग्राम होता है। नग्न आंखें इस तरह के छोटे कणों को नहीं देख सकती हैं। एक शक्तिशाली प्रकाश इलेक्ट्रॉन के साथ टकराकर और उसे प्रकाशित करके मदद कर सकता है। मदद करने के दौरान, इलेक्ट्रॉन की गति बदल सकती है, और उसका स्थान और गति का सटीक मापन नहीं किया जा सकता है।
उदाहरण के लिए, यदि हम एक इलेक्ट्रॉन के स्थान को इसके आकार (10^-10m) के साथ सटीकता से मापते हैं, तो इसकी गति के मापन में त्रुटि इसकी वास्तविक गति के बराबर या उससे अधिक होगी, यानी 10^6m/s या 1000 किलोमीटर/सेकंड के बराबर।
संक्षेप
हाइज़नबर्ग की अनिश्चितता सिद्धांत का आदान-प्रदान क्वांटम भौतिकी में कणों के स्थान और गति को सटीकता से मापने की असंभावना सूचित करता है। यह सिद्धांत हमें यह दिखाता है कि हम किसी कण के स्थान और गति को एक साथ पूरी तरह से निर्धारित नहीं कर सकते हैं, और हमें इन मापनों में एक निश्चित त्रुटि होनी है।
यह सिद्धांत क्वांटम मैक्रोस्कोपिक पदार्थों के मापन पर प्रभाव नहीं डालता है, लेकिन सूक्ष्म कणों के मापन पर प्रभावकारी होता है और हमें उनके स्थान और गति को सटीकता से मापने में कठिनाइयों का सामना करना पड़ता है।